Bernhard
Peter
Influenza:
Mechanismen der Virusvermehrung
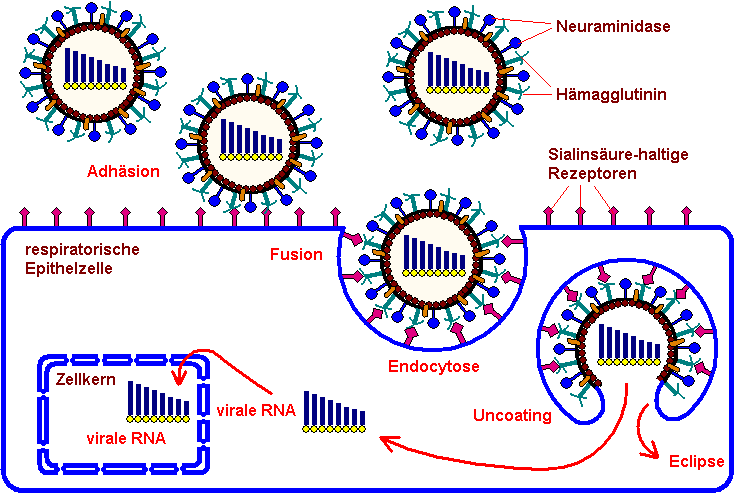
Rezeptorvermittelte
Endocytose
Nach der
Übertragung z. B.
durch Tröpfcheninfektion gelangen die Viren auf die Mucosa des
Respirationstraktes. Sie sind in der Lage, die Mucin-Schicht zu
durchdringen und die Epithelzellen zu infizieren. Die
Influenza-Viren verfügen mit dem Oberflächen-Antigen
Hämagglutinin über einen Erkennungsmechanismus:
Zellen auf den
Oberflächen (Epithelien) der Schleimhäute des
Respirationstraktes verfügen über Rezeptoren
(Glykoproteine und
Glykolipide), die Sialinsäure enthalten. An diese Rezeptoren
dockt das Hämagglutinin an und veranlaßt dadurch die
Aufnahme
der Viruspartikel durch rezeptorvermittelte Endocytose: Die
Zellmembran stülpt sich ein, umschließt das
Viruspartikel und
schnürt sich schließlich von der Doppellipidmembran
ab.
Membranfusion,
Uncoating und Eclipse
Das
Hämagglutinin induziert
Membranfusion, so daß das Innere des Virions in das
Zell-Lumen
gelangen kann. Für die Membranfusion ist ein niedriger pH-Wert
(pH 5) notwendig, der mittels des tunnelförmigen Ionenkanales
aus je vier Matrixproteinen M2 durch Einstrom von Protonen
aufrechterhalten wird. Das Hämagglutinin bildet Trimere, und
verschiedene Trimere bilden eine Fusionspore. Voraussetzung
dafür ist eine Spaltung des Hämagglutinins durch
zelluläre
Proteasen, die in der Regel bei der Reifung der Viruspartikel
erfolgt. Durch den erniedrigten pH-Wert kommt es zu einer Reihe
von sterischen Umordnungen beim Matrixprotein M1 und beim
Hämagglutinin. Eine hochlipophile fusiogene Domain
(Fusionsprotein) wird dadurch beim Hämagglutinin freigelegt,
die
sich in der lysosomalen Membran verankert. Dadurch kommen sich
beide Membranen näher. Das Endosom öffnet sich durch
Fusion der
Membranen und gibt den Inhalt des Viruspartikels ins Zell-Lumen
frei (Uncoating): helikale Ribonukleoproteine, zusammengesetzt
aus RNA und Polymerasen, also Informationsträger und ein
Enzym,
das diese Information zu vermehren in der Lage ist. Dieser
Vorgang ist ca. 20 – 30 Minuten nach dem ersten Anheften an
die Zelle abgeschlossen. Der Rest, die leere Virushülle, wird
in
der Zelle abgebaut und löst sich auf (Eclipse).

Produktion
neuer Virus-Bausteine
Die virale
RNA wandert in den
Zellkern der infizierten Schleimhautzelle und zwingt die Zelle
von da aus, ihren Stoffwechsel umzustellen. Es wird nicht
länger
synthetisiert, was dem Eigentümer der Schleimhaut, also dem
Menschen nützt, sondern was der Virusvermehrung dient. Zum
einen
wird durch die Polymerase die Virus-RNA vervielfältigt. Aber
die
Virus-RNA dient auch als Matrize, um die Eiweiß-Synthese der
Zelle umzustellen: Von ihr wird im Zellkern Boten-RNA, mRNA,
abgelesen, die an den zelleigenen Ribosomen die Produktion
viraler Eiweiße veranlaßt. Auf diese Weise wird die
Zelle
gezwungen, Matrixprotein M1, Nukleoproteine, Ionenkanäle M2,
Neuraminidase, Hämagglutinin, Polymerasen etc. herzustellen,
insgesamt 10 verschiedene Eiweiße, die alle zum Zusammenbau
neuer Virus-Partikel notwendig sind. Teile der viralen Proteine
fungieren dabei als Promoter. Einige der Proteine werden
unverändert verbaut, einige wandern in den Zellkern und binden
an die Virus-RNA zur Bildung neuer helikaler Nukleokapside,
andere Proteine werden im Golgi-Apparat prozessiert und mit
Zuckerresten versehen und dann über Membranfluß an
die
Zelloberfläche verbracht. Die Nukleokapside verlassen als
Ganzes
den Zellkern.
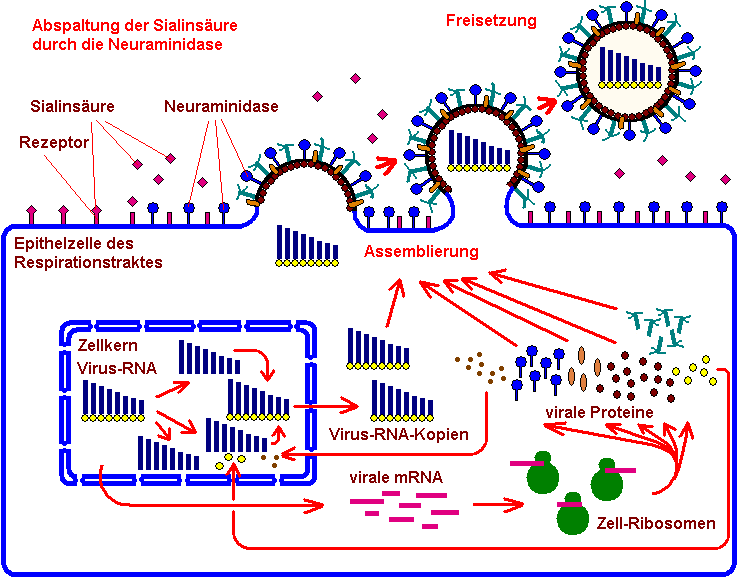
Assemblierung,
Reifung und Budding
Wenn alle
Bestandteile in
hinreichender Menge synthetisiert sind, kommt es zum Zusammenbau
neuer Virus-Partikel, der Assemblierung. Unter der Lipidmembran
der Zelle sammeln sich die Matrixproteine M1 und bilden eine Art
Halbschale, in der sich die Bestandteile sammeln. Diese neuen
Molekülaggregate werden zur Zelloberfläche
transportiert, wo
sie von einer Lipidmembran umschlossen werden und ausknospen und
sich schließlich als infektionstüchtige Viren
ablösen, um neue
Zellen zu befallen. Wichtig ist dabei, daß in die
betreffenden
Regionen der Lipidmembran, die zur Umschließung verwendet
wird,
alle benötigten Membranproteine und Glykoproteine eingebaut
werden, wie Neuraminidase und Hämagglutinin. In einer einzigen
Schleimhautzelle des Respirationstraktes können bis zu 100 000
neue Viruspartikel gebildet werden. Diese Knospung oder Sprossung
wird auch als „Budding“ bezeichnet.
Ein wichtiger Punkt ist auch die Reifung des Hämagglutinins: Voraussetzung für die Infektionsfähigkeit der neuen Virus-Partikel ist eine Spaltung des Hämagglutinins durch zelluläre Proteasen, die im betroffenen Gewebe, bei Influenza meist den Epithelien des Respirationstraktes, erfolgt. Die Frage, durch welche Proteasen sich das Hämagglutinin spalten läßt, entscheidet über den Gewebs-Tropismus der einzelnen Virus-Varianten.
„Freischneiden“
durch Neuraminidase
Ein ganz
entscheidendes Detail
fehlt noch: Wir erinnern uns, daß bei der
anfänglichen
Infektion die Kontaktaufnahme zwischen Hämagglutinin auf der
Virus-Oberfläche und dem Sialinsäure-haltigen
Rezeptor auf der
Zelloberfläche eine entscheidende Rolle gespielt hatte. In der
Tat müßte bei der Freisetzung das Gleiche passieren,
und die
neuen Viren würden mit der alten Zelle, die mittlerweile vor
dem
Exitus steht, verkleben. Um genau dies zu verhindern, ist die
Neuraminidase da: Die Neuraminidase wird vor der Knospung in die
Membran der Zelloberfläche eingebaut. Dort trennt sie
enzymatisch die Sialinsäure vom betreffenden Rezeptor ab. Das
geht, weil die Lipidmembran nicht statisch ist, sondern die
Moleküle in ihr in ständigem Fluß sich in
der Ebene bewegen
können. Nach der Abspaltung der Sialinsäure ist der
Weg frei,
die neuen Viren können nicht mehr an die Zell-Ruine andocken,
sie können sich ablösen und nach einer neuen Zelle
suchen. Und
wenn doch Viren an noch vorhandener Sialinsäure andocken,
werden
sie einfach durch die Neuraminidase abgeschnitten. Die
Replikation geht sehr schnell vonstatten: Nur 6 Stunden nach der
Erstinfektion werden schon neue Viren freigesetzt.
Das Freisetzen neuer Viren geschieht vorzugsweise am apikalen Ende der Epithelzellen, denn von dort aus können sich die Viren mit dem Luftstrom in den Atemwegen am besten weiter verbreiten.
Launenhafte Viren: Antigen-Drift und Antigen-Shift - Grippe-Medikamente - Neuraminidase-Hemmer - Literatur, Quellen und Links
Zurück
zur Übersicht Grippe /
Influenza
Andere pharmazeutische
Seiten
![]() Home
Home
©
Copyright Text, Graphik und Photos: Bernhard Peter 2006
Impressum